|
��
��
| |
��
|
�� ����
��ó�� ����
��(˼,
steel)�̶� �⺻������ ��(Fe)�� 2.0%������ ����(C)����
�ձ��� ���ϴ� ������, ���� ���� �� �������
���μ� ���� �θ� ���ǰ� �ִ� �ݼ�����̴�.
��� �ݼ������ ���귮 �߿��� ���� �����ϰ� �ִ�
������ �뷫 80% �����̴�. �̿� ���� ���� �θ�
���Ǵ� ������ �����ν� �������� ������ �پ��ϰ�
��ȭ��ų �� �ְ�, �� ����� ����(˭��, strength)��
�Բ� �Ҽ������� �����ϹǷ� ���ϴ� ������ ��ǰ����
�����ϱⰡ ���� �����̴�.
�� �ڵ����� ��ü�� ���Ǵ�
������ ������ ����Ͽ��߸� �ϴ� �ݸ鿡 ���������
���Ǵ� ���� ����� ��ȭ�Ǿ� �������� Ŀ�߸�
�Ѵ�. ���� �ڵ����� ���̳� ���������� �����緯 ��
���� ������ �μ�(����, toughness)�� ����Ͽ��� �Ѵ�.
���� �鵵���� ���� �浵�� ����ؾ߸� �Ѵ�.
�̿� ���� �ſ� ����
���ǿ������� ���� ���� �������� �̸������ ����
���� �پ��� �뵵�� ������ ������ ���߾� �ִ� ����
�־��� ���� ������ ��ó���� ���ؼ� �ַ� �̷������
�ִ�.
�Ϲ������� ���� ��ó���� �ǽ��ϴ� ������ ���� ����
�� ��� �Ѱ��� ������ ���ϱ� �����̴�.
�� ������
���Ͽ� ���� ������ �����Ѵٰų� �Ǵ� �ұ���
�ð��� ���� ������ �����ϱ� ���� ���̴�.
�� ���������� ���� ������������ �̼�ȭ��Ű�� ����
���̴�.
�� �ٶ����� ������������ �����ϱ� ���� ���̴�.
�� �浵�� ���ҽ�Ű�� ������ ����Ű�� ���� ���̴�.
�� �浵�� �������Ѽ� �������� ����Ű�� ����
���̴�.
�� ����� ��ݿ� �ߵ� �� �ֵ��� �μ��� ����Ű��
���� ���̴�.
�� �ǻ輺�� ����Ű�� ���� ���̴�.
�� �������� ����ɷ��� ����Ű�� ���� ���̴�.
�� ������ ������ ����Ű�� ���� ���̴�.
�� ���� �ڱ��� ������ �����ϱ� ���� ���̴�.
��
���� ���� ��ü���� ������ �� �������� �ֵ�
������ �� ���̰�, ���⼭�� �켱������ ����
��ó���� ���Ͽ� ���ϱ� ���� ���̶� �����̸�, ��
���� ���α����� ��� �̷���� �ִ����� ������
�˾� ���� ���� ������ �Ǹ��� �����Ѵ�.
|
|
�� ��(˼)�̶�
�����ΰ� ?
�� ź�Ұ���
Ư����
���
���� �⺻������ ö�� ź�ҷ� �̷���� �ձ��̶��
�θ��� ���� ���� �����ϴ�. �Ϲ������� 2.0%�� ������
ö����Ḧ ˼�̶� �ϰ�, 2.0%�� �̻��� ö����Ḧ
��ö(����, cast iron)�̶� �����ϰ� ������, 1.3��2.5%�ù�����
ö������ �ǿ뼺�� �����Ƿ� ���������� ����
�������� �ʰ� �ִ�.
���� ���� ź�Ұ�(����˼, carbon
steel)�� Ư����(���˼, special steel)���� �з��Ǵµ�,
���⼭ �츮�� ź�Ұ��� Ư������ ������ ��Ȯ�� ��
�ʿ䰡 �ִ�. ź�Ұ��� �⺻�����δ� Fe�� C�� 2���ձ�������
�Ϲ����� ź�Ұ����� C �̿ܿ� Si, Mn, P, S ����
�Ҽ����� �ҷ� �����Ǿ� �ִµ�, �̵� ���Ҵ� Ư����
� ������ ���ؼ� ÷���� ���� �ƴ϶� ���������߿�
�����̳� scrap���κ��� ȥ�ԵǾ��簡 �ƴϸ�
���ð������� ÷���� ���� �����ϴ� ���̱� ������
�̵� ���Ұ� �����Ǿ��ִ� ������ Ư�����̶�
�θ��� �ʴ´�. �� ���� KS�ݿ� ��豸����
ź�Ұ���� ������ SM 45C���� ��Ī������ 0.45C, 0.75Mn,
0.04P, 0.05S �� 0.22Si �̴�.
���� Ư������ ��Ȯ��
�����Ѵٴ� ���� ���� ���� �ƴ�����, �Ϲ������δ�
ź�Ұ������� ���� �� ���� Ư���� ������ ���
���Ͽ� 1�� �Ǵ� �� �̻��� �ձݿ��Ҹ� ÷����Ų ����
���Ѵ�. �� ���μ� �����θ������� Cr�� 12%�̻�
÷���Ͽ� ���ļ��� �����װ�, �ձݰ������� Cr, Mo,V
���� ���Ҹ� ÷���Ͽ� ������ ���Ҿ�
��ó��Ư���� ����Ų Ư������ �������� ���̴�.
|
|
�� ź�ҷ���
���� �з�
����
ź�Ұ��� �־ ������ ź�ҷ��� ���� ���� ������
������ ��ó������� �����DZ� ������ ���� �߿���
���Ҵ� ź���̴�. �̿Ͱ��� ź�ҷ��� �������� �߿伺
������ ź�Ұ��� �з��ϴ� �Ѱ��� ����� �ٷ� ��
ź�ҷ��� ���� �з��̴�.
�Ϲ������� 0.3wt% ������ ź�Ҹ�
�����ϴ� ź�Ұ��� ��ź�Ұ�(�����˼, low carbon steel)
�Ǵ� ����(��˼, mild steel)�̶�� �θ���, 0.3��0.6wt%��
ź�ҷ��� �����ϴ� ź�Ұ��� ��ź�Ұ�(������˼,
medium-carbon steel), ���� 0.6wt% �̻��� ź�ҷ��� ����
ź�Ұ��� ��ź�Ұ�(������˼, high-carbon steel)�̶��
�Ѵ�. ��ź�Ұ� �� 0.77%C �̻��� ź�Ұ��� Ư�� ������(����˼,
tool steel)�̶�� �θ���. ���� 1.3wt% �̻��� ź�Ҹ�
�����ϴ� ���� ��� �������� �����ϰ��� ����
������ �ʰ� �ִ�.
|
|
�� ��(˼)��
��ó��(������)
������
�ٿ� ���� ���� �뵵�� �پ��ϰ� �� ��뷮�� ū
������ ù°, ź�ҷ��� ���� ����������� �����ϰ�
��ȭ�ȴٴ� ���̴�. ǥ 1.1�� ��ö(0%C), 0.2%C�� ��
0.8%C���� ���ý�Ų ���� �������� ��Ÿ�� �����μ�,
ź�ҷ��� 0%���� 0.8%�� �����Կ� ���� �������� 4��
�̻� �����ϰ� �ִ� ���� �����ְ� �ִ�.
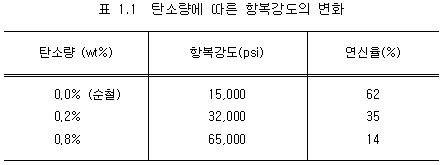
�̿Ͱ��� ���ý����� ��
ź�ҷ��� �����Կ� ���� ������ �������� ������
�ø�Ÿ��Ʈ(cementite : Fe3C)��� �Ҹ����
öźȭ���� ���� �����DZ� �����̴�. �� �� źȭ����
�ſ� ���ϱ� ������ �� �ӿ� �����ϰ� �Ǹ� ���� ��
�浵�� ����Ű�� �ȴ�.
���� �θ� ���Ǵ� �� �ϳ���
������ ��ó���� ���ؼ� �� ����������� �ſ�
�پ��ϰ� ��ȭ��ų �� �ִٴ� ���̴�. �� �ٸ�
�ݼ���ῡ ���ؼ� ��ó��ȿ���� �ſ� �����ϱ�
������ �� ��������� Ȯ��ǰ� �ִ� ���̴�. �� 1.1��
Fe-0.8%C���� 900�ɷκ��� �ð���ų �� �ð��ӵ��� ����
�������� ��ȭ�� ��Ÿ�� ������ �ð��ӵ���
�����ʿ� ���� �������� �ް��ϰ� �����ȴٴ�
����� �� �� �ִ�. �� �� 3���� �÷�� ������
ź�ҷ��� ���������� ��ó���� �ð������ ����
����������� ��ȭ�ϰ� �ִ�. �̿Ͱ���
�ð��ӵ��� ���� ������ �����Ǵ� ������ ����
���������� ��ȭ�DZ� �����ε�, ������ ���
�ݼ������ ����(Ư�� ���������)�� �� �ݼ���
���α����� ���� ���������� �����ϰ� �ִ�. �츮��
�� ���α����� ���� �̼�����(ڰ�����, microstructure)�̶��
���.
���� ź�Ұ��� ��� ������
ź�ҷ������� ��ó������� ���� �浵�� �����ϰ�
�����ٴ� ���� ��Ÿ���� �ִ�. ���� ź�ҷ���
��ó���� �������μ� �ʿ��� �浵 �� ������ �����ϰ�
���� �� �ִٴ� ���� �� �� �ִ�.
�ᱹ ��ó���� �Ѹ����
����ϸ� ���ʿ��� ������ ��� ���Ͽ� �ݼӳ�����
�̼������� ��ȭ��Ű�� ���� �� �ð����ۡ��̶��
���� �� �ִ�. ������ ���ϸ� �̼������� ��ȭ��
�������� �ʴ� ���� �� �ð������� �����������
��ȭ�� ���� ��Ÿ���� �����Ƿ� ��ó����� ���ϱ��
��ƴٴ� ���̴�.
|
|
��
ö �� ���� ��������
���
�ݼ��� Ư���� ���(������)�� �����ϰ���
��ü���¿��� ��Ģ���� ���ڹ迭�� �ϰ� �ִ�. �̰���
�ݼ��� �Ϲ����� Ư¡���� �ϳ��̴�. �����̶�
���ڰ� ��Ģ���� �迭�� �ϰ� �ִ� ���� ���ϸ�,
�ݼ��� ������ �ſ� �̽����� ���̹Ƿ� �������δ� ��
�� ���� X-������ �����ؾ߸� Ȯ���� �� �ִ�.
|
|
�� ö��
��������
��ö��
������κ��� �����ϸ鼭 �� ü����ȭ�� �����ϸ�
910�� �� 1390�ɿ��� ū ��ȭ�� �Ͼ�� ���� �� ��
�ִ�. �̰��� �� �µ��� ���� �Ͽ� �������ڰ�
���ڱ� ��ȭ�ϱ� ��������, 910�ɸ� A3������, 1390�ɸ�
A4�������̶�� �θ���. ��ö�� A3������ ������
�µ������� ü���Թ����(����ء۰̫��, body-centered
cubic : BCC)�� ���¸� ��Ÿ���µ�, �Թ�ü�� �� ������(8��)��
1����, ���� �Թ�ü�� �߽ɿ� 1���� ���ڰ� �����ϴ�
�����̴�. �̰��� �ݼ������п����� ����(��-Fe)���
���.
���� A3�������� A4������
������ �µ����� ��ö�� ����Թ����(����ء۰̫��,
face-centered cubic : FCC)�� ���¸� ��Ÿ���µ�, ��
���������� ���ڹ迭�� 8���� �������� ���� 1������
���ڰ� �����ϴ� ���� BCC�� ���������� ü�ɿ���
���ڰ� ���� �Թ�ü�� 6�� �߽ɿ��� ���� 1������
���ڰ� �����Ѵ�. �̰��� ����(��-Fe)�̶�� �Ѵ�.
���� A4������ �̻� ����(1534��)������ ���� BCC������
���ϴµ�, �̰��� ����(��-Fe)�̶�� �θ���.
�̿Ͱ��� ������ ������ ��� �µ��� ���� �Ͽ�
���������� ���������� �ٲٴ� ���¸� ���Һ���(����ܨ��,
allotropic transformation)��� �Ѵ�.
|
|
��
���Һ��½��� ü����ȭ
������
��Ÿ�� ������������ ����κ��� �� �� �ֵ��� BCC����������
������ ��ö�� FCC���������� ������ ��ö���� �е���
�۴�. �� ��ö�� ��ö���� ���� ������ ���ڹ迭��
�ϰ� �ִ�. ���Ƿ� ��ö�� ������κ���
�����ϸ� ����â�� ���ؼ� ü���� ��â�ϴٰ� 910�ɿ���
��ö�� ��ö�� �����ϸ� ���ڱ� ü���� �����ϰ� �ȴ�.
����ؼ� �����ϸ� ����â�� ���� ü����â��
����Ű�ٰ� 1390�ɿ��� ���� BCC������ ��ö��
�����ϸ鼭 �ް��� ü����â�� ����Ų��.
�ݴ�� 1390�� �̻���
�µ��κ��� �ð���Ű�� �� ������ ������ ��Ÿ����
�ȴ�. 1390�ɿ����� �ް��� ���� �� 910�ɿ�����
�ް��� ��â�� ��Ÿ����. Ư�� 910�ɿ����� �ް���
ü����â�� �ļ��ϴ� ��Ī��ó���� ���� �� �տ� ����
�������� ����Ű�� �⺻������ �ۿ��ϹǷ� ���ڵ���
�� ���� ���� Ư���� ���ذ� �ʿ��ϴ�.
|
|
�� ���� ����ü
����
ö�� ź���� �ձ��̹Ƿ� ö�� ���������� ƴ���̿�
�ҷ��� ź�Ұ� ������ ���·� �Ǿ� �ִ�. ��ö�̳� ��ö�̳�
��� ��ü�̰�, ��� ��üź�Ҹ� ������ ��
�����Ƿ� �̷��� ���¸� ����ü(ͳ����, solid solution)���
�θ���. ����ü���� 2������ �ִ�. �ϳ��� ��ſ�����
Fe ���� ���̿� ���� ���ڹݰ��� ���� ź�ҿ���(��������)��
�� �ִ� ħ���� ����ü(������ͳ����, interstitial
solid solution)�̰�, ���ϳ��� Fe ���ڳ��� Cr�̳� Ni��
���� ���� ���ڹݰ��� ����� ���ڰ� ��ſ�����
ö������ �Ϻθ� ��ġ�� ġȯ�� ����ü(������ͳ����,
substitutional solid solution)�̴�. ��ö�� ź�Ұ� ������
����ü�� �����Ʈ(ferrite), ��ö�� ź�Ұ� ������
����ü�� �����׳���Ʈ(austenite)��� �θ���.
�����Ʈ���� ź���� �����Ѱ�� ��¿��� 0.008%, 723�ɿ���
0.02%�� �ݸ鿡 �����׳���Ʈ���� ź���� �����Ѱ��
723�ɿ��� 0.8%, 1147�ɿ��� 2.0%�μ� �����׳���Ʈ �ӿ�
����� �� �ִ� ź�ҷ��� �ξ� ����.
ź�ҷ��� ���� ��������
�����Ʈ�� �����׳���Ʈ�� ���� �����Ѱ踦
�Ѿ�� Fe�� C�� ������ ���ں�μ� ���յ� ȭ�չ���
�ø�Ÿ��Ʈ(cementite : Fe3C)�� �����ȴ�. ��
�ø�Ÿ��Ʈ�� ź�ҿ��� ȭ�չ��̹Ƿ� źȭ���̶��
�ϸ�, ������ ����ü�ʹ� �ٺ������� �ٸ� ���̴�.
�� �����Ʈ�� �����׳���Ʈ�� ���� ����ü��
�Ϲ������� �µ��� ���� ���������� ź����
�����Ѱ谡 ��ȭ������ �ø�Ÿ��Ʈ�� ���
�µ������� �� �߷�%�� 6.67%(����%�δ� 25%)�� ź�Ҹ�
������ �ִ�.
�̿� ���� ���бݼӿ��ڵ���
���� ������ ������� ���յǰ�, ������ ����������
������ �ձ��� �ݼӰ�ȭ�չ�(����������ڪ, intermetallic
compound)�̶�� �ϸ�, �浵�� ���� �ſ� ����� Ư¡��
���� �ִ�.
|
|
�� ħ�����ڸ�(interstitial
site)
�����Ʈ��
�����׳���Ʈ�� �ᱹ ��� Fe���ڳ��� ź�ҿ��ڰ�
�����Ǿ� �ִ� ħ���� ����ü�̰�, ��ſ����� Fe���ڻ�����
ƴ�ڸ��� ź�Ұ� �����Ѵٴ� �͵� �˾Ҵ�. ����
���⼭ �츮�� ������ ź�ҿ��ڰ� �����ϴ� �ڸ���
������� �� �ʿ䰡 �ִ�.
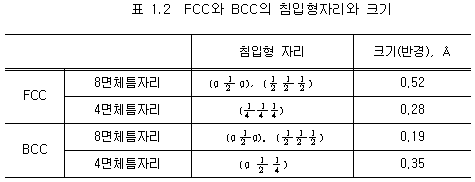
8��üƴ�ڸ��� 4��üƴ�ڸ���
ũ��� ū ���̰� �ִ�. ǥ 1.2�� FCC�� BCC��
ħ�����ڸ��� �� ũ�⸦ ��Ÿ�� ���̴�. ö������
������ �����̰� ���� ������ �ִٰ� ������ ��
�����׳���Ʈ(FCC)���� 8��üƴ�ڸ��� ũ��(�ݰ�)��
0.52��������, 4��üƴ�ڸ��� ũ��� 0.28�ʿ� �Ұ��ϴ�.
�� �����׳���Ʈ���� 4��üƴ�ڸ����� 8��üƴ�ڸ���
ħ�������ڰ� ħ���ϱ� ���ٴ� ���̴�. ����
ź�ҿ��ڴ� 8��üƴ�ڸ��� ���� ħ���� �� ������, ��
ƴ�ڸ��� ũ��(0.52��)���� ź�ҿ����� �ݰ�(0.7��)�� ��
ũ�� ������ ������â�� ���� ���� ����.
���� ǥ 1.2���� �� �� �ִ� �ٿ�
���� �����Ʈ������ ħ�����ڸ��� ũ���
�����׳���Ʈ�������� �ξ� �۴�. �� 8��üƴ�ڸ���
ũ��� 0.19��, 4��üƴ�ڸ��� ũ��� 0.35�ʿ� �Ұ��ϴ�.
�̿Ͱ��� BCC������ �����Ʈ���� ħ�����ڸ���
ũ�Ⱑ �۱���� �����׳���Ʈ���� ź�Ҹ�
�����ϱⰡ ���������. ���� �� ������ �����
�ٿ� ���� �����Ʈ���� ź���� �����Ѱ��
�����׳���Ʈ�������� �ξ� ���� ���ۿ� ���� ���̴�.
���� �����׳���Ʈ�� 8��üƴ�ڸ�(0.52��)��
�����ϴ� ���� ź�ҿ��ڰ� ���ÿ� BCC�� 8��üƴ�ڸ�(0.19��)��
���� �ְԵǸ� ���ں����� ���� �� ���� �Ǿ� �ᱹ
�Թ�������(cubic structure)�� ����������(tetragonal
structure)�� ���ϰ� �ȴ�. �̷��� �ؼ� ������
������ �츮�� �����ٻ���Ʈ(martensite)��� �θ���,
���� ��ȭ��Ű�� ���� ��ó���� �ñ����� ������ �ٷ�
�� �����ٻ���Ʈ������ ������Ű�� ���� ���̴�.
|
|
�� ������
�ݼ���
���������� ���� �̽����� ũ���� �����̹Ƿ�
���̰��� ���ؼ��� �� �� ���� X�� ȸ���� ���ؼ� ��
���¸� Ȯ���� �� ���� ���̴�. ���� �ݼ���
�Ѹ��� ���(����)���·� ������ �� ����Ż(nital)��
���� ������ �νĽ�Ű�� ������ ������ �� �ִ�. ��
������ ���� ������ ���� ���� ���ڵ��� ��
�ݼ��� �̷�� �ִٴ� ���� �� �� �ִ�. ��
�ϳ��ϳ��� ���ڸ� ������(̿��أ, grain)�̶� �ϰ�,
���������� ��踦 ��������(̿��أͣ, grain boundary)���
���.
�� ������
��������
�� ������ ����������
�ʱ�ܰ迡���� ���� "������"�� ������
�ְԵǴµ� ��ü�� �µ��� �������� �������ڸ���
����� �Ϻο����� �� �������� �����DZ� �����Ѵ�.
������ �������� �����ϸ鼭 �����῭��
����ǰ�, �� ���� �ܺη� ���Ǹ鼭 �������� �ᱹ
������ ������ �ε�ĥ ������ ��� �����Ѵ�. �̷���
������ �������� ���������� ���ڹ迭�� �ұ�Ģ����
ũ��, �̶��� �ұ�Ģ���� ������ ����ʿ� ����
�ܷ���� ����Ǵ� �������Ұ� ���������� ����
Ŀ����. �������谡 ���� ���νļ��� ���� ����
������ �ٷ� �̷��� ������ �ұ�Ģ�迭�� ���� ���̴�.
���� ��������� �ݼ����о߿��� �ϳ��� ����(�����)����
�з������� ������ �����Ǵ� ������������� �ſ� ū
������ ��ģ��.
��
������ũ��� ���������
������ũ��� �ݼ��� ����,
�Ҽ��� � ���ؼ� ������ �´�. �� 1.10�� �ʹ�
��ö, �δ� ��ź�Ұ��� �����Ʈ������ ������ ����(100��)��
��Ÿ�� ������, ź�Ұ� �ҷ� ������ ��ź�Ұ���
�������� �ξ� �̼��ϴٴ� ���� �� �� �ִ�. ����
������ũ��� �ð��ӵ����� �����ϴµ�, �Ϲ�������
�ð��ӵ��� Ŭ���� �������� �̼�������.
�̷��� �������� ũ� ����
����������� ���� ������ �ִµ�, �����°�
������ũ����� ���̿��� ������ ���� �������
�����ȴ�.
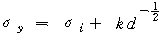 (5-10) (5-10)
���⼭ 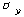 =
������ =
������
 = �Գ����� ������ �̵��� �����ϴ� ��������
= �Գ����� ������ �̵��� �����ϴ� ��������
 = ���
= ���
 = �������� ����
= �������� ����
�� ���� Hall-Petch ������̶� �ϴµ�,
��κ��� ������ ����� �������� ������ũ�Ⱑ
�̼��Ҽ��� �����Ѵٴ� ���� ��Ÿ���� �ִ�. �̿Ͱ���
�������� �̼��Ҽ��� �ݼ��� �������Ӹ� �ƴ϶�
�Ƿΰ��� �� �μ��� �����ǹǷ� ������
�ݼ����о߿��� �������� �̼�ȭ�� �ſ� �߿���
��������� ����å���� �̿�ǰ� �ִ�.
|
|
�� Ȯ��
������
�ٿ� ���� ��ó���� �ݼӳ��� ���¸� �����Ѽ�
����������� ������ �����ϴ� ���۹���̴�. ����
���� ��ó���� ��Ÿ���� ���´� �ļ��ϴ�
�����ٻ���Ʈ���¸��� �����ϰ��� ��� Ȯ����
�����ϴ� �����̹Ƿ�, ��ó���� ���� �����������μ�
Ȯ�꿡 ���� �⺻������ �ľ��ϴ� �͵� �ſ�
�߿��ϸ��� �����ȴ�.
�Ϲ������� ���̳� ������ ��� ������
������ �����ϸ� �� ������ ������ �κ����κ���
����� �κ����� �̵��ϰ� �Ǵµ�, �̰��� Ȯ��(��ߤ,
diffusion)�̶�� �Ѵ�.
|
|
�� Ȯ��ⱸ(mechanisms
of diffusion)
����
������ �ݼӳ����� ���ڵ��� ��� �̵��ϴ°�? �̿�
���� �ⱸ�μ��� ���������� ������ ���⼭�� ����
�Ϲ����� �ⱸ�� ħ���� Ȯ��ⱸ(��������ߤѦϰ,
interstitial mechanism)�� ���� Ȯ��ⱸ(������ߤѦϰ,
vacancy mechanism)�� ���ؼ��� �˾ƺ���� �Ѵ�.
�� ħ�����ⱸ
��� ħ�����ڸ��� ��ġ�ϴ�
ħ�������ڰ� ��ſ��ڵ��� ��ġ�� ��ȭ��Ű�� �ʰ�
������ ħ�����ڸ��� �̵��ϴ� �ⱸ��
ħ�����ⱸ��� �Ѵ�. �� 1.1(a)�� FCC ������ (100)
�鿡���� ħ�������ڸ� ��Ÿ���� ���̴�. ħ��������
1�� ħ�����ڸ� 2�� �̵��ϱ� ���ؼ��� ��ſ����� 3��
4�� �ణ�� �ٱ������� �̵��Ǿ�߸� �Ѵ�. ��
ħ�������ڰ� ������ ħ�����ڸ��� �̵��ϱ� ����
��ΰ� ���õǾ�߸� �Ѵ�. �̿� ���� ��ֹ���
�غ��Ǵ� �ӵ��� �ᱹ ħ���������� Ȯ��ӵ���
�������ִ� ���̴�.
���� �� ħ�����ⱸ�� ���ؼ�
Ȯ���Ϸ��� �ϴ� ���ڴ� ��ſ��ڿ� ���ؼ� ũ�Ⱑ
�۾ƾ߸� �����ϰ�, �����ε� ź��(C)�� ����(N)�� ����
���� ũ�Ⱑ ���� ħ���������� Ȯ���� �� �ⱸ��
���ؼ� �̷������ �ִ�. �� ������ �Ͼ�� ź����
�̵��� �������� ħ����Ȯ���̶� �� �� �ְ�, ��
ħ�����ⱸ�� ���� Ȯ���� �ļ��ϴ� �����ⱸ�� ����
Ȯ�꺸�� ���� �����ϰ� �Ͼ��.
�� �����ⱸ
����µ� 0oK(-273��)����
�ݼӰ����� �������ڿ� ������ ���ڰ� �迭�� ���·�
�Ǿ� �ִ�. ���� �µ��� ����ϸ� ���ڰ�
���������κ��� ����Ǿ� ����ִ� �������� �����
�ȴ�. �̿Ͱ��� ���ڰ� ����Ǿ� ����ִ� ��������
����(����, vacancy)�̶�� �Ѵ�.
�� ������ ������ � ���ڰ�
�������� �����Ͽ� �̵��� �� �����ⱸ�� ���ؼ�
Ȯ���ϰ� �ִٰ� ���Ѵ�. �� 1.1(b)�� FCC ���ڿ���
������ ������ ���ڰ� �������� �����Ͽ� �̵��ϴ�
������ �����ִ� ���̴�. ���������� �� �� �� 1��
���ڿ� 2�� ���� ������ ������ 0.73�̹Ƿ� �־���
���ڰ� ���� ȭ��ǥ�� ���� ������ �������� �̵���
�� �䱸�Ǵ� 1�� ���ڿ� 2�� ������ ������ �״���
ũ�� �ʴ�. ������ �ұ��ϰ� �����ⱸ�� ���ؼ�
Ȯ���ϴ� ö���ڰ� ħ�����ⱸ�� ���ؼ� Ȯ���ϴ�
ź�ҿ��ڿ� ���ؼ� �ξ� ������ Ȯ���ϴ� ������
ź�ҿ��� �������� ħ�����ڸ��� �� ����������
ö���� ������ ������ ������ Ȯ���� ����ϱ�
�����̴�.
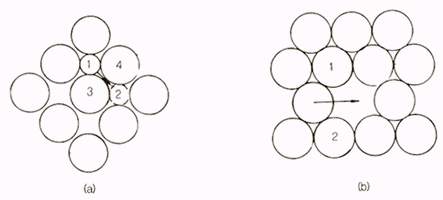
�� 1.1
Ȯ��ⱸ�� ������
(a)
ħ�����ⱸ (b) ġȯ���ⱸ
|
|
�� Ȯ���� �̿�
������
�ٿ� ���� ���� ��ó���� ���¸� ����Ű��
���۹���̰�, ���� ���� ���´� ��Ȯ�꺯��(����ߤܨ��,
diffusionless transformation)�����ٻ���Ʈ���¸���
�����ϰ��� Ȯ���� �����ϴ� Ȯ�꺯��(��ߤܨ��,
diffusional transformation)�̹Ƿ� �ſ� �߿��� �����̴�.
Ư�� ǥ���ȭó��������μ� �ſ� �θ� ���Ͽ�����
�ִ� ħź(����, carburizing)�̳� ��ȭ(����, nitriding)ó����
Ȯ�������� ���� �̿��ϴ� ����̹Ƿ� ��������
���������� Ȯ���� ���������� �� �߿伺�� �ſ� ũ��.
�̿ܿ��� ����(��ȿ �Ǵ� ���۸���), Ȯ��Ǯ��(����ȭǮ��)
�� ���������� � Ȯ��� ���������� ���õǴ�
�����̴�.
|
|
�� Ȯ�꿡
������ �ִ� ����
Ȯ�꿡
������ ��ġ�� ���ڴ� ���������� �ִ�. ù°��,
�µ��� �������� ���� ������ �������� Ȱ�������Ƿ�
Ȯ��ӵ��� ������ �ǰ�, �� ���������� �ִ� ��쿡
Ȯ���� �����ϰ� �Ͼ��. Ư�� �����̳�
÷�������� ������ �翡 ���� Ȯ��ӵ��� ��ȭ�ȴ�.
���� ��� ��ö���� ��ö���� ź�Ұ� Ȯ���ϴ�
���� �� �����ϴ�.
|
|
�� ���¿� ����
�� ���¿�
������
�ϻ��Ȱ����
���Ǵ� ���¶� ���ʹ� �� �ݼӿ����� ���۽���
��ȭ �� �ݼ��� ���������� ��ȭ�Ǵ� ���� ����(ܨ��,
transformation)��� �Ѵ�. ��ö�� �����ϸ� ��ö�� ������
��â�ϴٰ� ��� �µ�(A3������)�� �����ϸ� ���ڱ�
������ ����Ű�� �ȴ�. �� ���۽��� ��ȭ(����)��
������ ���������� ��ȭ�� ���ؼ� �Ͼ�� ���̴�.
���¸� ����Ű�� �µ��� ������(ܨ����, transformation
temperature)�̶�� �θ���.
|
|
�� ���� 5����
����
��������
A0, A1, A2, A3 �� A4�� 5���� ���°� �ִ�. ���߿��� A3���´�
��ö(ü���Թ����)
��----�� ��ö(����Թ����)
910��
����
��Ÿ�����µ�, ������ �ٿ� ���� ���������� ��ȭ�ȴ�.
A1, A4���µ� ���������� ��ȭ�̴�. ���� �̵� ���´�
��ü ������ ���ڹ迭�� ��ȭ�� �����Ѿ߸� �ϹǷ�
���¿µ��� ������ �ణ �ʷ��Ѵ�. A3�������� ����
��� �������� �������� Ac3, ���� �������� Ar3��
ǥ���Ͽ� �����Ѵ�. ÷�� c �� r�� �Ҿ��� chauffage (����),
refroidissement (�ð�)�� ù���ڸ� ��Ÿ����.
A2���´� ��ö�� �ڼ��� �Ҵ�
����, A0���´� �ø�Ÿ��Ʈ�� �ڼ��� �Ҵ� ���¸�
���Ѵ�. �̵� ���´� ���������� ��ȭ�� ��������
�����Ƿ� ���������� ��ȭ�� �����ϴ� ������ ���¿�
�����ؼ� �ڱ⺯��(��Ѩܨ��, magnetic transformation)���
�Ҹ�������. ���� ��Ī�� ���� �ļ��ϴ� �ٿ� ���� A��
����� Ar', Ar''�̶�� �ϴ� ���°� �ִ�.
|
|
�� ���¿�
������ȭ
���´�
���������� ��ȭ�̹Ƿ� ���������� �� ���̰�������
���Ѵ�. ���� �������� ù���ڿ��ٰ� start(����)��
ù������ s�� �ٿ��� ���°��ÿµ��� ��Ÿ����, finish(����)��
ù������ f�� �ٿ��� ��������µ��� ��Ÿ����. ����
��� ������ ����.
Ms
: �����׳���Ʈ �� �����ٻ���Ʈ���� ���°���
Mf : �����׳���Ʈ
�� �����ٻ���Ʈ���� ��������
Ps : �����׳���Ʈ
�� ����Ʈ���� ���°���
Pf : �����׳���Ʈ
�� ����Ʈ���� ��������
����
��ó���� ���谡 ���� ���´� Ư�� A1�� A3���·μ�,
�ļ��ϴ� ö-ź�Ұ� ���µ��� ź�ҷ��� ���� ��������
��ȭ�� �����μ� ��Ÿ�� ���̴�.
|
|
�� ź�ҿ�
�ձݿ����� ����
�� ���� ������
ź��
��
������ ���� �з��� �� ź�ҷ��� ���� ��ź�Ұ�,
��ź�Ұ� �� ��ź�Ұ����� �з��Ͽ����� ������ ����
�з��ϴ� ����� �ִ�.
�ؿ���
------------ 0.2%C ����
�� ��
------------ 0.2��0.3%C
�ݰ氭 ------------
0.3��0.5%C
�� ��
------------ 0.5��0.8%C
�ְ氭 ------------
0.8��1.5%C
ź�Ұ�
ö�߿��� ȭ���ϸ� �ø�Ÿ��Ʈ(Fe3C)��� �ϴ�
źȭ���� �����Ǵµ�, �� �ø�Ÿ��Ʈ�� ��Ŀ�� �浵 HV=1100������
�ſ� ���� ȭ�չ��̴�. ������ 1%�� ź�Ҵ� 15%�� Fe3C��
�����ϹǷ� �̰��� ź�Ұ� ���� ���ϰ� �ϴ� �����̴�.
���� ��Ī�浵�� ź�ҷ���
�����Կ� ���� Ŀ������ �̰��� 0.6%C������ �ش�Ǵ�
���̰�, �� �̻� ź�ҷ��� �����ص� ��Ī�浵��
�������� �ʴ´�. �� 1.2�� �̰��� ��Ÿ�� �����μ�,
�� 0.6%C������ ź�ҷ��� ���� ��Ī�浵�� ����������
�� �̻� ź�ҷ��� �����Ͽ��� HRC 65 �̻����δ� ����
�ʴ´�.
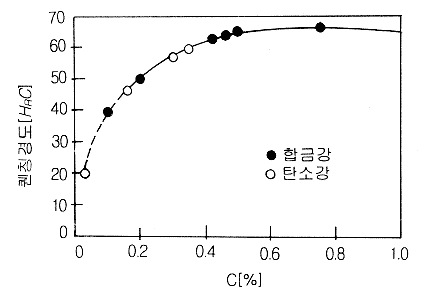
��
1.2. ���� ź�ҷ��� ��Ī�浵���� ����
|
|
�� ź�ҷ���
������ ��ȭ
ź�Ұ���
������ �⺻������ ź�������� ���ؼ� �����Ǹ�,
ź�ҷ��� �����ص� �������³� ��ó�����ǿ� ����
�� ������ �����ϰ� ��ȭ�ȴ�. ���������� ǥ�ػ�����
ź�Ұ��� ������ ���ؼ��� �����ϱ�� �ϰ�, �����̳�
��ó���� ���� ������ȭ�� ���� �忡�� �����ϱ��
����.
�켱 ǥ�������̶�� �ϴ� ����
ź�Ұ��� ��3 �� ��cm �µ� �̻� 30��50�ɷ� �����Ͽ�
������ �����׳���Ʈ�� ���� �� ������� ����������
���� �����Ǵ� �������μ�, �ư�����������
�����Ʈ�� ����Ʈ, ������������ ����Ʈ, ����
�������������� �ø�Ÿ��Ʈ�� ����Ʈ�� �ȴ�.
�� ������
������ ȭ���� ����
������
�ٿ� ���� ���� �����Ʈ�� �ø�Ÿ��Ʈ(Fe3C)�μ�
�̷���� ȥ�������� ���� �ְ�, �� ������
ȥ�պ����� ź�ҷ��� ���ؼ� �����DZ� ������
ź�Ұ��� ������ ������ ź�ҷ��� ���� ����������
��ȭ�ȴ�.
�� 1.3�� ź�Ұ����� ź�ҷ���
���� ������ ������ ��ȭ�� ��Ÿ�� ���̴�. ������
���� ź�Ұ��� ����, ����â��� �� ����������
ź�ҷ��� �����Կ� ���� ���ҵ�����, ��,
�������� �� ���ڷ��� �����ȴ�.
���� ź�Ұ��� ���ļ��� ź�ҷ��� �����ɼ���
�����ϰ�, �ҷ��� Cu�� ÷���Ǹ� ���ļ��� ���ȴ�.
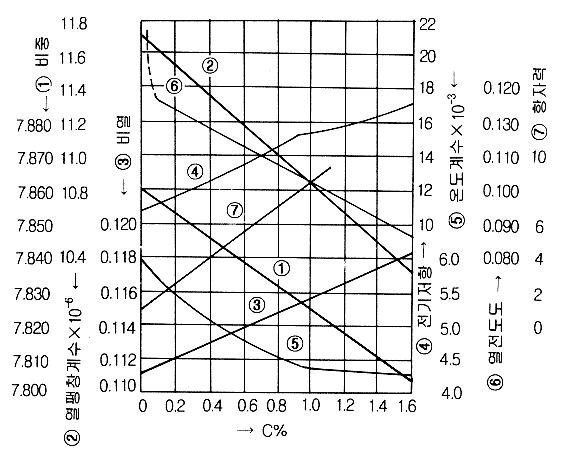
��
1.3. ���� ������ ������ȭ
�� ��� �����
����
ź�Ұ���
ź�����(Young's modulus) E�� 20000��22000������2,
������(shear modulus) G�� 7700��8450������2, Poisson��
�� ���� 0.28�μ� �̵� ������� ź�ҷ��� �������
���� �����ϴ�. ���� �� 1.4���� ���� �ٿ� ����
�ٸ� ����� �������� ź�ҷ��� ���� ����������
��ȭ�Ǵµ�, �ư����������� ���尭��, �浵 ��
���� ���� ź�ҷ��� ���� �����ǰ�, ������ ��
�ܸ鰨������ ź�ҷ��� ���� �����Ѵ�.
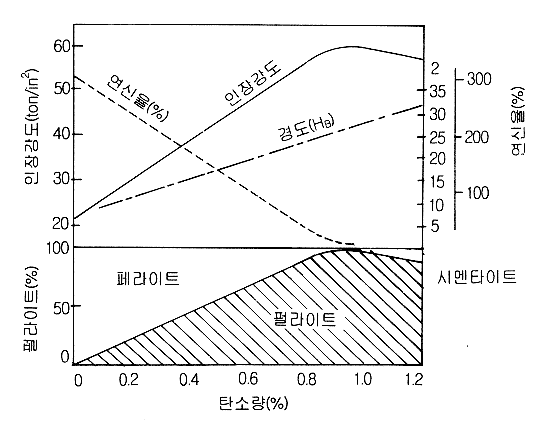
�� 1.4.
ź�Ұ��� ����� ���� �� ������ ����
��������������
�ø�Ÿ��Ʈ�� �������� ��Ÿ���Ƿ� ź�ҷ���
�����Կ� ���� ���尭���� ������ �����Ѵ�. ����
�浵�� ����ؼ� �����ȴ�.
���� �̿� ���� ź�ҷ��� ����
����� ������ ��ȭ�Ǵ� ���� ǥ 1.3�� ��Ÿ��
�����Ʈ, �ø�Ÿ��Ʈ �� ����Ʈ�� ����� ������
���õǾ� �ִ�. �� �����Ʈ�� ���� ������ ũ��
���尭���� ���� �۴�. ���� �ø�Ÿ��Ʈ�� �ſ�
�浵�� ���� ����Ͽ� �μ��� ���� ������,
����Ʈ�� �����Ʈ�� ���ؼ� ���尭���� ũ��
�浵�� ����. ���� �ư��������� ź�ҷ��� ����
���尭�� �� �浵�� �����Ǵ� ���� ����Ʈ����
������ �����Ѵٴ� ���� ǥ�κ��� ������ �� �ְ�,
���� ������������ �������� �����ϴ� ���� ��������
���� 0 �� �ø�Ÿ��Ʈ �����̶�� ����� �� �� �ִ�.
�̰��� �� 1.4�� �ϴܺο� ź�ҷ��� ���� �����Ʈ,
�ø�Ÿ��Ʈ �� ����Ʈ�� ���� ������ ����� ������
���ý��Ѻ��� ���� �� �� �ִ�.
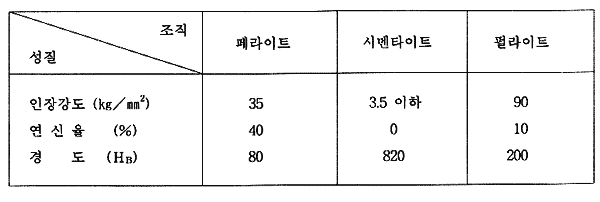
ǥ
1.3 �����Ʈ, �ø�Ÿ��Ʈ �� ����Ʈ�� ����� ����
�� ���� ����� ����
����
������ ź�Ұ��̶� �µ��� ���� �� ����� ������
�ſ� ������. �� ���μ� 0.25%C�� �ư��� ź�Ұ���
������ 0��500�� ���̿��� �Ͼ�� �������� �����
������ ��ȭ�� �� 1.5�� ��Ÿ�´�.
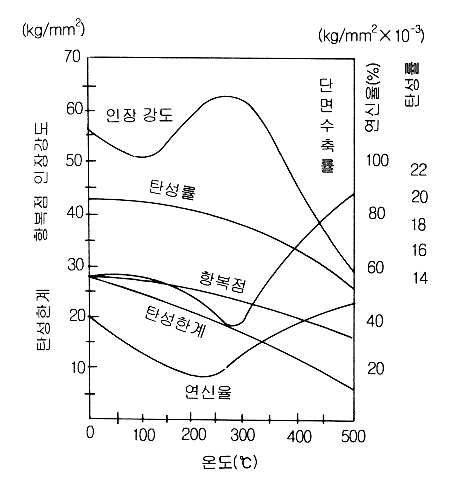
��
1.5. �µ��� ���� ź�Ұ��� ����� ����
������
���� �ٿ� ���� ź�����, ź���Ѱ� �� ���� ����
�µ��� ����Կ� ���� �����Ѵ�. ���� ���尭����
200��300���� �µ����������� �����Ͽ� �ִ밡 �ǰ�,
�������� �ܸ鰨������ �µ���¿� ���� �����ϴٰ�
���尭���� �ִ�� �Ǵ� �µ����� �ּҷ� �ǰ��� ����
�ٽ� �����ȴ�.
���ġ�� 200��300�ɿ��� ����
�����Ƿ� ź�Ұ��� �� �µ��������� ���� ����ϰ�
�ȴ�. �̰��� û���뼺(��������, blue brittleness)�̶�
�ϸ�, �� �µ��������� �����ϴ� ���� ���ϴ� ����
����.
��� ������ �µ������� �µ���
���ϵʿ� ���� ���尭��, �浵, ź�����, ���� ��
�Ƿ��Ѱ� ���� ���� ����������, ������, �ܸ������
�� ���ġ ���� ���ҵǾ� ������ ���������. ���ġ��
�µ����Ͽ� ���� �����ϴٰ� � �Ӱ�µ�, ��
õ�̿µ�(������, transition temperature)�� ���Ǹ�
�ް��� ���ҵǾ� -70�� �αٿ����� ���� 0 �� �����
���� ���´�.
|
|
�� �ձݿ���
÷���� ���� ���� ���� ��ȭ
˼�߿���
����(�˼)�������� ���� �������� ����Ű�� ����
���Ƿ� ÷���� �ձݿ��ҵ� ������, �� �̿ܿ� ��ö(����),
scrap ���� ����κ��� ȥ�ԵǴ� �̷��� �ܷ����ҵ�
�����ϴµ�, �̷��� �ܷ����ҵ��� ���� ������ ��ġ��
��� ������ �� ����. �̷��� �ܷ����ҵ� �߿��� Cu,
Ni, Co, Sb, As, W, Mo, Sn ���� �����ÿ� ���� ������ ��
���� ���ҷμ� ���� ġȯ������ �������ְ�, ����
������ ��ȭ��Ű�� ���ؼ��� ���� �ٷ�÷����
�ʿ��ϴ�. ���� C, H, N ���� ���ҵ��� ������ �Ϻ�
������ �� �ִ� ���ҵ�μ�, ���� ħ��������
�����ؼ� �̷�����ε� ���� ������ ū ������ ��ģ��.
���� ���������� ���� ������ �������� ���ҵ���
���� �������� ��ġ�� ������ ����Ͽ� �����Ͽ���.
(1) ź��(C)
ź�Ҵ� ���� ������
����Ű�µ��� ���� ȿ�����̰� �߿��� ���ҷμ�,
�����׳���Ʈ�� �����Ͽ� ��Ī ��ó����
�����ٻ���Ʈ ������ ������Ű�� �Ѵ�. ź�ҷ���
������ �Բ� ��Ī�浵�� ����Ű���� ��Ī��
�������߰��ɼ��� ũ�� �Ѵ�. Fe, Cr, Mo, V ���� ���ҿ�
ȭ���Ͽ� źȭ���� �����ϹǷν� ���� �� �浵��
����Ų��.
(2)����(Mn)
ź�Ұ����� ���� 0.35��1.0%
������ Mn�� �����Ǿ� �ִ�. �� Mn�� �Ϻδ� �� �ӿ�
����Ǹ�, �������� �� �ӿ� �����Ǿ� �ִ� S��
�����Ͽ� ��ݼӰ��繰(nonmetallic inclusion)�� MnS��
���������� �����ϴµ�, �� MnS�� ������ �־ �Ҽ������ÿ�
������������ ��� ���ŵȴ�. ���� �� MnS��
�������ν� �� ���� S�� ���� ���ҵǹǷ� �������迡
�����Ǵ� ����ϰ� ������ȭ�չ��� FeS�� ������
������Ų��.
���� Mn�� ���ؼ� ����Ʈ��
�̼�������, �����Ʈ�� ���밭ȭ��Ű�Ƿν�
ź�Ұ��� �������� ����Ų��. �� ��Ī��
��ȭ���̸� ������Ű����, ���� ���� �����Ǿ� ����
������ ��Ī�տ��̳� ������ ���߽�Ų��. ���� Mn��
���� ������ �ο��ϹǷ� 1.0��1.5%Mn�� ÷���� ����
���ΰ�(˭��˼)�̶�� �θ���, Ư�� 1.3%C, 13%Mn��
������ �����׳���Ʈ���� Hadfield˼�̶�� �θ���
�����κ��� ������ ���̴�. �� Mn�� ���� ���꼺(ұ߫��)
�� ����ȭ��(ұ߫����)�� �����ϴ� �����̴�.
(3) Ȳ(S)
�� �ӿ� �����Ǿ� �ִ� S�� ����
Mn�� �����Ͽ� MnS ���繰�� �����Ѵ�. ���� �� ����
Mn ���� ���ġ ���� ������ Fe�� �����Ͽ� FeS��
�����ϱ �ϴµ�, �Ϲ������� �� FeS�� �������迡
��������� ����Ǿ� �ִ�. �� FeS�� �ſ� ����ϰ�
�������� ������� ���� �� �ð������ÿ� �տ���
����ų �� �ִ�. ���� �طο� FeS ���繰�� ������
���ϱ� ���ؼ��� Mn:S�� �� ���� 5:1�� �ϰ� �ִ�.
�Ϲ������� Mn, Zn, Ti, Mo ���� ���ҿ� �����Ͽ� ����
�ǻ輺�� ������Ų��.
(4) ��(P)
P�� �� �ӿ� �����ϰ� �����Ǿ�
������ �������� ������, ���� Fe3P�� �طο�
ȭ�չ��� �����Ѵ�. �� ȭ�չ��� ���� ����ϰ�
�����Ǿ� �־ Ǯ��ó���� �Ͽ��� ����ȭ���� �ʰ�
����, �п� ���� ������ �ϸ� ��� �þ��.
��������� ���Ͻ�Ű��, ���۸��뼺�� �����ϸ�, ��
��谭������ �ǻ輺�� ������Ű�� ���ҷ� ��dz�,
�Ϲ������δ� �Ҽ����μ� ���ֵȴ�.
(5) �Լ�(Si)
�� ���� Si�� ��ö�� Ż��������
�ܷ��Ǵ� ������, SiO2 �� ���� ȭ�չ���
�������� �ʴ��� �����Ʈ �ӿ� ����ǹǷ� ź�Ұ���
������������� ū ������ ��ġ�� �ʴ´�. ���� P��
���� Ż�����̰�, 4.5% ÷���������� ������
����Ű���� 2% �̻� ÷���ÿ��� �μ��� ���Ͻ�Ű��
�Ҽ��������� ��ġ�Ƿ� ÷������ �Ѱ谡 �ִ�. ����
���۸��� ��ȭ������ �����Ű�� ȿ���� �ִ�.
(6) ����(N)
�� �߿� �ܷ��ϴ� ���ҷ���
���ؿ���, ���ع���� ���� �����ϰ� ��ȭ�ȴ�.
�Ϲ������� ���Ҵ� ���� �̷� ����ε� ����
����������� ū ������ ��ġ�µ� ���尭��,
�������� ������Ű��, �������� ���Ͻ�Ų��. Ư��
���ġ�� ���� �� õ�̿µ��� ����� �����ϴ�.
���Ҵ� ź�ҿ� �����ϰ� ħ���������̰�, ���߿���
Ȯ��ӵ��� ������, ���� �����Ʈ�� ���ؼ� �ִ� ��
0.1%(580��)��� 0.003%����(���)���� ����������
���ص���ȭ�� ��Ÿ���� �� �ٸ� �ܷ����ҿʹ� Ʋ����
ū Ư¡�� �ִ�. �̶����� ���� ������ �뼺�̳�
��ȿ��ȭ���� ��Ÿ����. ��Ī�ÿ� �Ͼ�� ��Ī��ȿ(quench
aging), �ð������� ���� ������ȿ(strain aging), ����
200��300�ɿ����� û���뼺�� ���ؼ� ���� ���尭��,
�������� �����ϰ� ���ġ�� �����ؼ� ���� ��ȭ��
����Ų��. Ư�� �ؿ��� ������ deep drawing �����ÿ�
ǥ�鿡 �ָ��� ���ϴ� ������ �ַ� ������
������ȿ�� ���� ���̴�. �̰��� ����ȭ��Ű��
���ؼ��� ���ҿ� ģȭ���� ū Al, Ti, Zr, V, B ����
÷���ϹǷν� �̵��� ��ȭ������ �����Ѵ�. �� ���Ҵ�
�ٸ� �ձݿ��ҿ� �����Ͽ� ��ȭ���� �����ϹǷ� ����
���������� ������ ��ģ��. AlN�� ���߿� �̼��ϰ�
����Ǿ� ������ �����׳���Ʈ�� �������� �̼��ϰ�
�Ǿ� ������(�أ˼)�� ������ �����ϰ�, �̿ܿ� Ti, Zr,
V, Nb � ��ȭ���� �����Ͽ� �������� �̼��ϰ�
�����. ���� AlN�� �ٷ� �����ϸ� �����μ���
ũ�� ��ġ��, Ư�� �����ÿ��� �����׳���Ʈ �迡
AlN�� �����Ͽ� ���뼺�� ����Ų��. ���� AlN��
��� ���� ����ũ���������� ���ϵȴ�.
(7) ����(H)
���Ҵ� ���ڹݰ��� ����
�����Ƿ� Fe�����߿� N, C ��� �����ϰ� ħ��������
����Ǿ� �ְ�, ���߿����� �ٸ� ���ҿ� ���ؼ�
Ȯ��ӵ��� �ſ� �����Ƿ� ������ �������� �̵��� ��
�ִ�. �� ���Ҵ� ����(����), ��� ũ��(hair crack), ����
����(��������) �� ������ ��� �տ� �� ��������
������ �������� �ȴ�. �̷��� ������ ���� �Ǵ�
���Ÿ� ���Ͽ� �ֱٿ��� �������� �Ǵ� ����ó����
���� Ż���Ҹ� ���ϰ� �����Ƿ� ������������ ����
���ҿ� ���� ������ ���ҵǰ� �ִ�.
(8) ���(O)
��Ҵ� ���� Fe�� �������
�ʱ���� ���߿����� �ַ� ��ݼӰ��繰�μ�
�����ϸ�, �̵��� SiO2, Al2O3, Cr2O3,
TiO2 ���� Fe�� ���ؼ� ���뵵�� ���� ������
FeO, MnO ���� ���¿��� �ణ �����Ѵ�. Ư�� �̵�
��ݼӰ��繰�� ���� ���������, �Ƿ�Ư�� ����
���Ͻ�Ų��. ������ ���� Fe-O �ձݿ�����
����������� ������ �Բ� ���õ�̿µ��� �����ϰ�
���������, ��ö�� �ҷ��� C, Mn ���� �����ϸ� ��
������ ���� �������. ��Ҵ� �ٷ����� �����Ǿ�
������ ���� ħź�� �̻������� �������� �ʰ� ���ÿ�
��ȭ���� ���Ͻ�Ű��, ������ ���� �����׳���Ʈ
�������� ������ ������Ų��.
(9) ����(Cu)
Cu�� ���� ������� ����
ȥ�ԵǹǷ� ������ ���� 0.1��0.3% ���� �����Ǿ� �ִ�.
Cu�� ��¿��� �����Ʈ�� 0.35%���� �����Ͽ�
���밭ȭȿ���� ��Ÿ���Ƿ� ���� �� �浵�� �ణ
������Ű���� �������� ���Ͻ�Ų��. Cu�� ������
�������� ������������ ������ �Ǵµ�, Ư�� 0.5%�̻�
�����Ǿ� ���� ������ �����뼺(��������, red
brittleness)�� �������� �ȴ�. �̰��� ���°����ÿ� Fe����
Cu�� ��ȭ�ӵ��� �����Ƿ� ��ǥ�鿡 �����Ͽ�
���������߿� ���� ���η� ħ���ϱ� ����������, Ni�̳�
Mo�� ÷���μ� �� ������ ������ ������ �� �ִ�. ����
Cu�� ���� �ҷ� �����Ǿ� �־ ��� �� �ؼ��߿���
���� ���ļ��� �����ϰ� ����Ų��. Cu�� P�� ������
��� ���ļ���� ���� ȿ�����̴�.
���� 0.4%Cu �̻� ÷���ÿ��� Cu��
�̼���� ���� �����ȭȿ���� ��Ÿ���Ƿ�, ������
�����θ����������� Cu�� 4%���� ÷��������Ѽ� ����
�����θ������� ����� �ִ�.
(10) �˷�̴�(Al)
Al�� ��Ż�����μ� ��ȿ�ϳ�
÷������ ������ ���� ����ϰ� ������ Ż��,
Ż�������μ��� 0.1%���Ϸ� ÷���ϴ� ���� �����̴�.
��ȭ���� AlN�� �̼������Ͽ� ���� �������̼�ȭ��
ȿ�����̹Ƿ� �̰��� �̿��ؼ� �ع̼� �������� ����
���ΰ��� ������ �� �ִ�. ���� ���»�ȭ���� ��
����ȭ��(ұ�����)�� ���� ȿ�����̴�.
(11)
���(As)
As�� ����������������
�����ϴ� ���� ���� �Ұ����ϰ�, �� ������
��������� ���ؼ� As�� ���������� ÷���ϴ� ����
���� ���ٰ� ���Ƶ� ����. �� As�� 0.2%���� �̻���
���ġ�� �����ϰ� ���Ͻ�Ű��, ���õ�̿µ���
��½�Ŵ�� �Բ� ���� ������������ ��ġ��
�����뼺�� ����Ų��. ���� �̷��� �ǿ�����
���밭�� �����Ǿ� �ִ� ������ As�������� ����
������ ���� �ʴ´ٰ� ���Ƶ� ����.
(12)
�ؼ�(B)
�̷� ÷��(0.0005��0.003%)�μ�
��ȭ���� ������ ������Ų��. ���� ÷���Ǹ� Fe3B��
�����Ͽ� �����뼺�� ����Ų��.
(13)
�ڹ�Ʈ(Co)
��κ��� �ձݿ��Ҵ�
�ҷ�÷���ν� ���� ��ȭ���� ����Ű���� Co��
���ܷμ� �� �ݴ��� ������ ��Ÿ����, �� �����̹Ƿ�
�Ϲ����� ������ ������� �ʰ� �ڼ�, �����������,
������� � ÷���ؼ� ������ �����ϴµ���
����ϰ� �ִ�. Ư�� ���� ���°����� �����ϴµ���
ȿ�����̴�.
(14)
ũ��(Cr)
13%���� ÷���μ� �����׳���Ʈ
������ Ȯ���Ų��. �����̰�, �ٷ� ÷���ص� ��ȭ��
����Ű�� �ʴ� źȭ���� ������Ų��. 10%�̻� ÷���ϸ�
�����θ��������� �ǰ�, ����ȭ���� ����Ű��
����ȭ���� �����ϹǷ� �����밭, ������,
�����θ����� �� �������� ���� ���ο� �����Ǿ� �ִ�
���� �߿��ϰ� �������� �ձݿ����̴�. �� Cr÷������
���� �Ǹ� ����̶�� �ϴ� ���ڼ��� ����� ����
��Ÿ����. Cr�� ���� �����뼺�� �����뼺�� �����ϴ�
ȿ���� ������ ���۸��뼺�� �����Ѵ�.
(15)
�����굧(Mo)
Mo�� 0.1��0.3%������ ÷���μ� Ni��
10����� ��ȭ���� ����Ű�� ȿ���� �����Ƿ�
���۸��뼺�� �����Ͽ� ���۸���ȭ������ �ο��Ѵ�.
���� źȭ���� �����ϹǷ� �������������
�ձݿ��ҷε� ����� ȿ���� ��Ÿ����,
����������ȭ�µ��� ��½�Ų��. ��ȭ�ɿ� ���ؼ���
Mo �ܵ����ٴ� Cr�� �����ϸ� ���� ȿ�����̴�. ����
��δ�.
(16)
����(Ni)
Ni�� ���� ������ �̼�ȭ��Ű��,
�����׳���Ʈ�� �����Ʈ���� ������ �ߵǹǷ�
������ ��ȭ��Ų��. �� Cr�̳� Mo���� �����ϸ� �����
��ȭ���� ��Ÿ���� ���������� ��ó���� �����ϰ�
�Ѵ�. Ni�� �����׳���Ʈ ����ȭ�����̹Ƿ� Cr����
�������� �����׳���Ʈ�� �����θ�����, ��������
�����Ѵ�. ���� �����μ��� ������ ������Ű�� ������,
���ܼ�(ʦӴ��)�� ��ġ�� �ʴ´�. ���� Ni�� C�� N��
Ȯ���� ������ �ϹǷ� �������� ��ȭ(����)��
�����ϰ�, ��â��, ������, ������(������) ����
�������� Ư¡�� �ִ�. �� Fe-36%Ni���� ��ºαٿ�����
����â����� 0�� �����Ƿ� �������(������) ��
Ư�����μ��� �뵵�� �д�. ���� Ni�� Cr�� �Բ�
���� �߿��ϰ��� �������� �ձݿ����̴�.
(17)
ƼŸ��(Ti)
Ti�� O, N, C, S �� H �� ���
���ҿ͵� ���� ģȭ���� ��Ÿ����, Ư�� Ż��, Ż��(����)
�� Ż��(���)�� ���� ���ȴ�. źȭ�������ɵ� Cr����
���ϰ�, �������� �̼�ȭ��Ű�����
�����θ������̳� ����������� ������ �̿�ȴ�.
���� Ÿ�ݼӿ��ҿ͵� ȭ�չ��� �����Ͽ�
�����ȭȿ���� �����ϹǷ� �����ȭ��
�����θ������̳� �����ڼ� � �̿�ȴ�.
(18)
�ּ�(Sn)
Sn�� scrap���κ��� ȥ�ԵǾ�
�������������� ���� ���ŵ��� ���ϴ� ���ҷμ�,
�����Ʈ���� �� 8%���� �����Ѵ�. �Ϲ������� Sn��
���� ���尭��, �������� ������Ű��, ������,
���ġ�� ���ҽ�Ű�� �� P�� ����� ������ ����
������ P��ŭ ���������� �ʴ�. ���� Sn��
������������ �����뼺, ���۸��뼺, �����뼺 ����
�������� �ǰ�, ���ļ��� �ణ�� ������ �ֱ��
������ �Ϲ������� ������ ������ �����̴�.
(19)
������(Se)
Mn ��� ȭ�չ��� �����
�ǻ輺�� ����Ų��. ��Ȳ���� �ξ� �����̸� �밭(��˼)��
�������� ���� �Ѵ�.
(20) Į��(Ca)
������ Ż�����̴�. �밭�߿���
��ȭ�Ͽ� �����ϱ� ����Ƿ� Ca-Si, Ca-Si-Mn ���� ���·�
÷���Ͽ� ��ݼӰ��繰�� ���� �� ������ ������
���Ѵ�.
(21) �Ͽ���(Nb)
������ ������ �̼�ȭ���ҷμ�
������ ����ȭ�µ��� ��½�Ų��. ��ȭ����
���Ͻ�Ű��, ���۸��뼺�� ���ҽ�Ų��.
(22) �ڷ��(Te)
���� �ǻ輺�� �����Ű��,
������������ ��ģ��.
(23) ��(Pb)
���� �ǻ輺�� ����Ų��.
(24) �ٳ���(V)
źȭ�� �������� Ŀ��
�̸�źȭ���� ����� ���� ������ �̼�ȭ��Ű�Ƿ�
����°����κ��� ���� �������� �̸������ ����
���ǰ� �ִ�. ���۸���ȭ������ Mo�̻����� ����.
���°����� ���� ����Ű���� ��ȭ���� V2O5��
������� ���Ƽ� ���������ϹǷ� ÷������ �Ѱ谡
�ִ�.
(25) �ֽ���(W)
W�� �����̰�, ������ Ŀ��
�����ϱ� ����Ƿ� �����밭���� ���� ÷������
������, ��ȭ���� ����Ű�� Fe4W2C
�Ǵ� Fe3W3C���� źȭ���� �����ϹǷ�
������ Ư�� ����������� �̿�ǰ�, 18%W-4%Cr-1%V����
���ӵ������μ� �����ϴ�. �� W�� ������ �ڼ�����
�ִ�.
(26)
������(Zr)
N, S, C �� H���� ģȭ���� Ti���� ����
���ϱ���� �̵� ������ ������ ���� �̿�ǰ� �ִ�.
������ ���� 0.2��0.3%÷���� ������ ������ ��
�ִٰ� �˷��� �ִ�.
��������
1.
����ټ, �����, ����, ������ : �������, Ѧ���ϼ��,
1994
2. ʰ�� ΰ : �䪵���� ��������������������,
��������, 1981
3. G. Krauss : Principles of Heat Treatment of Steels,
American Society for Metals, Metals Park, Ohio, 1980
4. C. R. Brooks : Heat Treatment of Ferrous Alloys,
McGraw-Hill, New York, 1979
5. ������������������ : �����������(��),
����������ڤ��, 1970
6. P. G. Shewmon : Diffusion in Solids, McGraw-Hill, New
York, 1963
7. C. R. Barrett, W. D. Nix, and A. S. Tetelman : The
Principles of Engineering Materials, Prentice-Hall, New
Jersey, 1973
8. L. E. Samuels : Optical Microscopy of Carbon Steels,
American Society for Metals, Metals Park, Ohio, 1980
9. ��������������������������� :
������������������, ����������ڤ��, 1961
10. P. M. Unterweiser, H. E. Boyer, and J. J. Kubbs : Heat Treater's
Guide, American Society for Metals,
Metals Park, Ohio, 1982
11. C. S. Barrett and T. B. Massalski : Structure of Metals, 3rd Ed. McGraw-Hill,
New York,
|
�� |